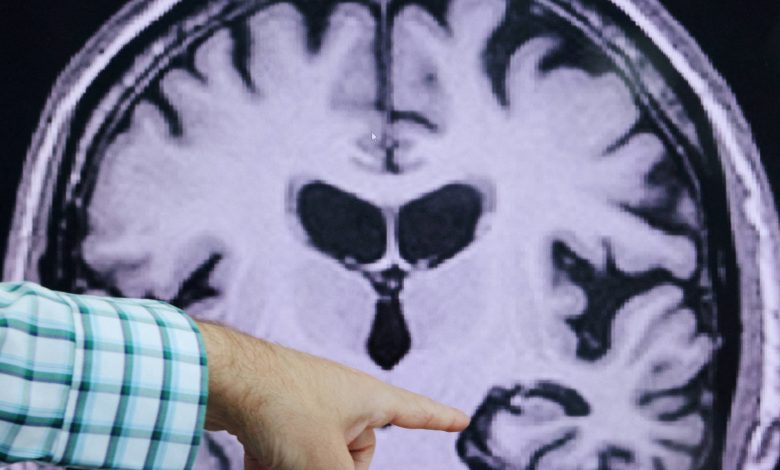
Decisão da FDA sobre tratamento experimental para Alzheimer
No dia 10 de maio, os conselheiros externos da FDA concluíram de forma unânime que os benefícios do tratamento experimental para Alzheimer da farmacêutica Eli Lilly, o donanemab, superam os riscos. O comitê de especialistas concordou que os dados do ensaio clínico mostraram a eficácia do medicamento em pacientes com estágio inicial da doença.
Essa decisão abre caminho para a aprovação final da FDA sobre o novo tratamento. Inicialmente prevista para este ano, a agência convocou a reunião com seus conselheiros externos para obter uma visão especializada antes de seu veredicto.
Dawn Brooks, líder de desenvolvimento da Lilly para o donanemab, expressou sua satisfação com o reconhecimento do forte benefício do medicamento pelo comitê consultivo. A empresa agora aguarda a revisão final da FDA, que geralmente segue as recomendações de seus especialistas independentes.
Aspectos únicos do ensaio
A FDA destacou alguns aspectos únicos do ensaio da Lilly em comparação com outros tratamentos aprovados anteriormente. O donanemab e o Leqembi, produzidos por Eisai e Biogen, têm o objetivo de remover placas tóxicas de beta amiloide no cérebro de pacientes com Alzheimer em estágio inicial.
A diferença principal no desenho do ensaio da Lilly foi a medição dos níveis de uma proteína chamada tau, associada à morte de células cerebrais. Esse critério permitiu a seleção de pacientes mais propensos a responder positivamente ao tratamento dentro do período de 76 semanas do ensaio.
O ensaio clínico mostrou que o donanemab foi capaz de retardar a progressão dos problemas de memória e pensamento em 29% dos participantes, resultado comparável ao observado com o Leqembi.
Apesar dos benefícios, questões de segurança foram levantadas, especialmente para pacientes com duas cópias do gene APOE4, associado a um maior risco de Alzheimer. O voto do painel foi importante no processo de aprovação, preparando o terreno para uma eventual decisão da FDA.
Agora, com o aval positivo do comitê consultivo, a Eli Lilly planeja expandir seus estudos para incluir pacientes geneticamente predispostos ao Alzheimer, como aqueles com síndrome de Down.
A expectativa dos analistas é de que a FDA aprove o donanemab, o que seria um avanço significativo no tratamento da doença neurodegenerativa. As ações da Eli Lilly fecharam em alta após a votação, refletindo a confiança dos investidores na possível aprovação do medicamento.




